Edition 25 février 2014
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Questions fréquemment posees
|
|
|
|
|
|
SAM_GC dans la suite intrumentale SAM
|
|
SAM_GC est un des trois instruments qui constituent la
suite instrumentale SAM, les deux autres étant le
spectromètre de masse quadrupolaire (QMS)
développé par le NASA/GSFC, et le spectroscope laser
accordable (TLS) développé par le NASA/JPL. Ces trois
instruments sont intégrés dans une structure incluant
l'échantillonneur de l'expérience constitué de
77 fours placés sur un carroussel. Ce sytsème permet
d'amener chacun des fours dans une position dans laquelle ils peuvent
être remplis par des échantillons de sols ou de roches
prélevés par Curiosity, puis de les amener à une
position dans laquelle il peuvent être chauffés
jusqu'à 1100°C.
|
|
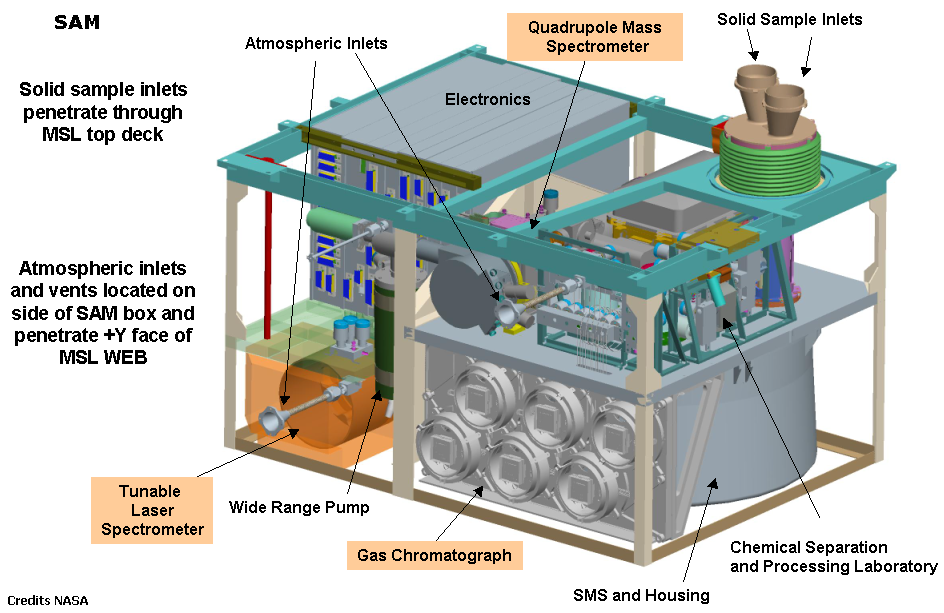
Représentation
de la suite instrumentale SAM
|

Le modèle de vol de SAM GC
intégré dans la structure mécanique de SAM au NASA
GSFC (janvier 2008)
|
|
Objectifs scientifiques et analytiques de SAM_GC
|
|
L'objectif de SAM_GC est principalement l'analyse et
l'identification des molécules organiques et inorganiques issues
du traitement des échantillons de sol prélevés par
Curiosity. Deux types de traitement seront appliqués aux
échantillons, à savoir un chauffage progressif depuis la
température ambiante (~0°C) jusqu'à environ
1100°C, et un
traitement chimique qui doit permettre à des molécules
organiques importantes mais non volatiles, de pouvoir être
vaporisées et analysées par la suite instrumentale. Dans
les deux cas, il est fort probable que plusieurs espèces
gazeuses soient relachées par l'échantillon. Si ces
espèces sont nombreuses, leur injection directe dans le
spectromètre de masse ne permettrait pas de les identifier
individuellement car leurs signatures spectrales se recouvriraient,
rendant le traitement du spectre très difficile. L'utilisation
en amont du chromatographe en phase gazeuse (GC) permet de
séparer les
composés présents dans le mélange gazeux et de les
injecter individuellement (dans le cas idéal) dans le
spectromètre de masse (QMS). Ainsi le traitement des spectres de
masse et l'identification des molécules est possible et
fortement facilitée. Le chromatographe doit également
permettre, dans une certaine mesure, l'identification des
espèces analysées. En effet, le temps que mettent les
espèces analysées à traverser le système GC
est caractéristique de l'espèce analysée et des
conditions d'analyse. Ce temps, appelé temps de
rétention,
pemet donc d'identifier de manière indirecte les composés
analysés. L'analyse simultanée avec le
spectromètre de masse permettra donc d'obtenir deux informations
qui seront croisées afin d'identifier les composés, ce
qui sécurisera
leur identification.
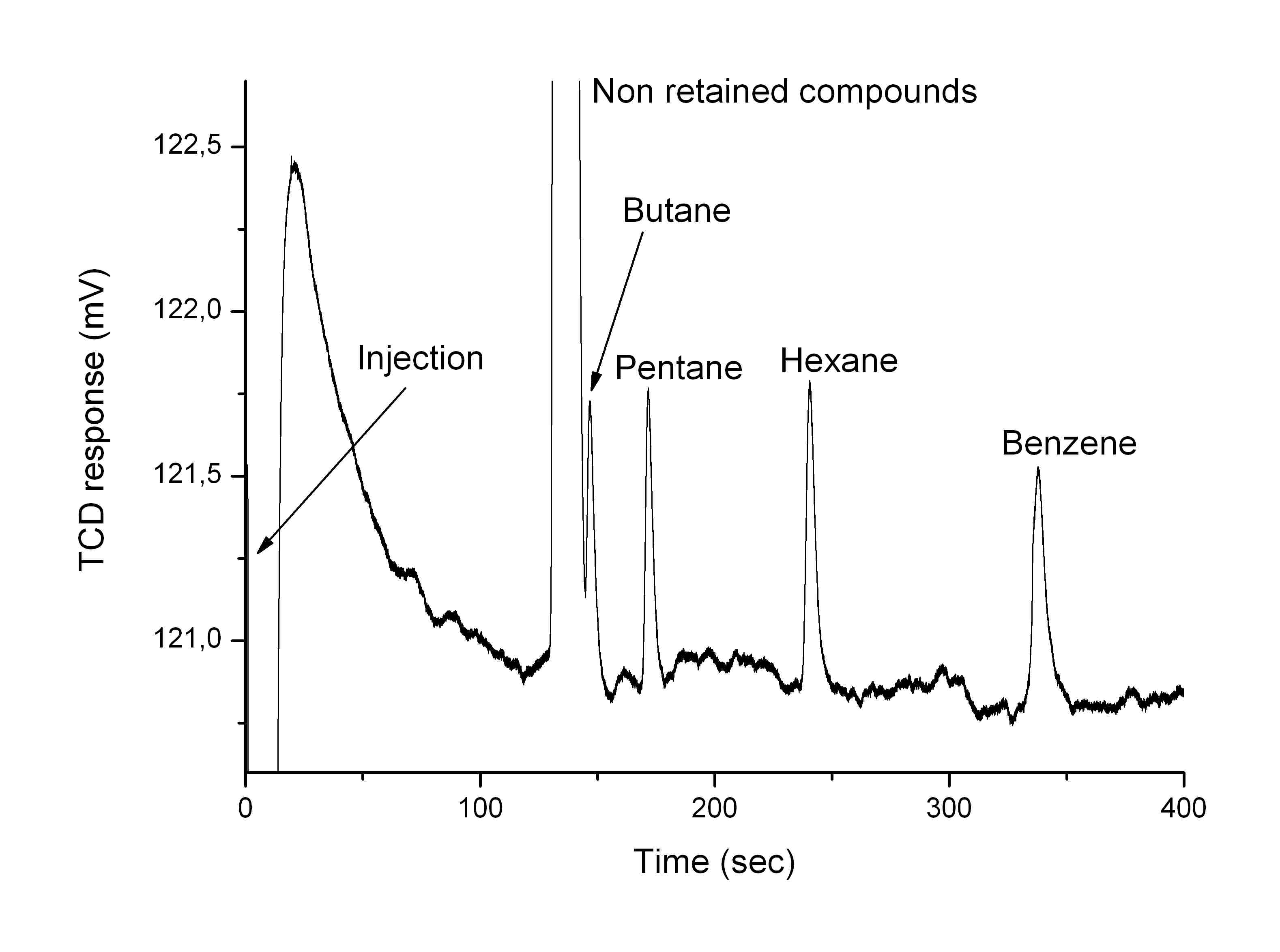
Exemple d'un
chromatogramme de molécules
organiques et de l'argon. La
séparation est matérialisée dans le
temps, qui correspond au temps passé
par l'espèce chimique dans le chromatographe
|
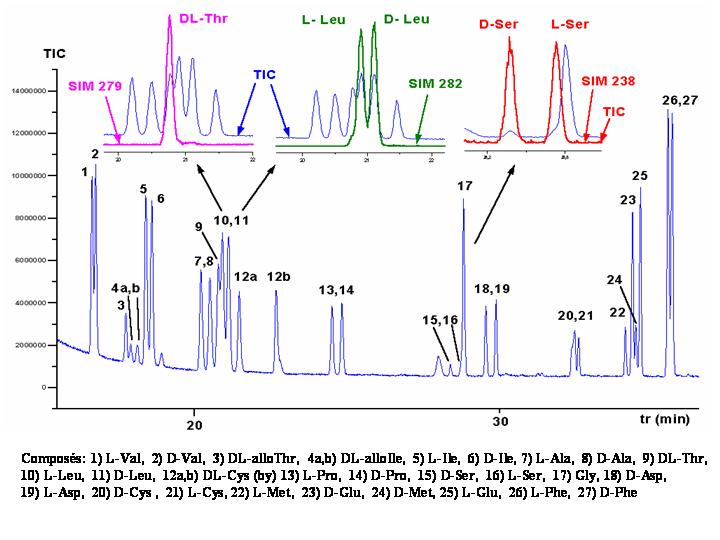
Exemple de séparation des
énantiomères de différents acides aminés
par chromatographie en phase gazeuse. Les énantiomères
d'une espèce chimique sont dénomés L ou D en
fonction de la géométrie
de la molécule
|
Le chromatographe permet également l'analyse des
énantiomères, ce que ne peux pas faire le QMS tout seul.
En effet, des énantiomères sont des molécules
disymétriques identiques en composition et en structure
chimique, mais qui sont l'image l'une de l'autre au travers d'un
mirroir. Cette différence n'est pas détectable avec un
QMS et actuellement, seules des méthodes de séparation
(comme la chromatographie) ou des méthodes optiques permettent
de la mettre en évidence. La quantification du rapport de la
quantité des deux énantiomères d'une
molécule est aujourd'hui très importante du point de vue
de l'exo/astrobiologie puisque les molécules qui constituent le
code génétique du vivant (tel que nous le connaissons)
sont des molécules homochirales, c'est à dire qu'une
seule des deux formes énantiomérique est
utilisée. Les acides aminés, par exemple, sont
utilisés sous la forme dite "L" alors que les sucres sont
utilisés sous la forme dite "D". L'origine de cette
homochiralité est aujourd'hui inconnue mais on sait qu'elle est
uniquement liée au vivant. Par conséquent, la
détermination du rapport énantiomérique des
molécules organiques présentes à la surface de
Mars pourrait être un moyen, soit de mettre en évidence
une
activité biologique ou prébitoique, soit de mettre en
évidence des mécanismes physico-chimiques qui pourraient
être à l'origine de l'homochiralité du vivant sur
Terre.
Pour finir, SAM_GC aura également pour
objectif secondaire de procéder à l'analyse et la
séparation des espèces atmosphériques, afin de
remonter aux propriétés de l'atmosphère et
également obtenir des informations sur l'histoire de Mars et de
son atmosphère.
|
Description technique
|
|
Pour répondre aux objectifs scientifiques, SAM_GC
est composé de six voies analytiques, chacune dédiée
à la séparation d'une gamme précise de
composés potentiellement présents dans les
échantillons analysés. Ces six voies incluent chacune une
colonne chromatographique (tube capillaire) et un dispositif permettant
de les maintenir à température stable entre l'ambiante
(environ 30°C) et 250°C.
La colonne est le lieu de la
séparation des espèces chimiques analysées. La
paroi interne des tubes est
recouverte d'une substance active qui possède une
affinité spécifique à chaque espèce
chimique. Cette substance peut être soit un adsorbant (un solide
qui interagit avec les espèces en créant des liaisons de
Van der Waals. Plus une espèce a d'affinité avec
l'adsorbant et plus elle passe de temps dans la colonne) soit une
résine
(une substance visqueuse dans laquelle les espèces chimiques
peuvent se dissoudre. Dans ce cas, il existe un échange entre la
phase gazeuse et la phase "dissoute" pour chaque espèce chimique
analysée. Une espèce qui a une forte affinité avec
la résine passera plus de temps sous forme dissoute. Sous cette forme,
les espèces progressent plus lentement le long du tube que sous
forme gazeuse. Les espèces ayant une plus grande affinité
seront donc celles qui passeront le plus de temps dans la colonne). Les
adsorbants sont plutot dédiés à la
séparation des très petites molécules (e.g. N2,
CO, CH4...) alors que les résines sont plutot dédiées
à séparer les molécules organiques, ce qui inclut
les énantiomères.

Photo d'une colonne chromatographique métallique.
La colonne est
longue d'environ 30 m et son diamètre mesure
approximativement 0,25 mm. Sur l'incrustation en haut à gauche,
on voit une photo prise par microscopie électronique à
balayage de la sortie d'une colonne. On distingue sur le bord
intérieur du tube la phase stationnaires déposée
(ici, un adsorbant)
|
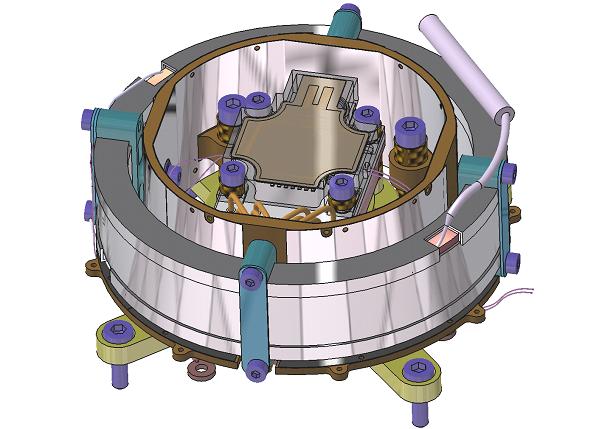
Schéma d'un module analytique de SAM GC.
Sur le dessus, on
voit le détecteur TCD. Le cylindre métallique
extérieur est la structure qui
contient la colonne
|
Cinq des six voies analytiques sont équipées
d'un détecteur à conductibilité thermique (TCD)
qui mesure la différence de capacité des gaz qui sortent
de la colonne à conduire la chaleur, comparativement
au gaz vecteur. Le gaz vecteur est un gaz inerte (ici l'hélium)
qui est injecté dans la colonne chromatographique à
vitesse constante et qui entraine avec lui l'échantillon gazeux.
Lorsqu'un composé sort de la colone, il est
mélangé au gaz vecteur, ce qui modifie la
conductibilité de la chaleur du gaz, et c'est cette variation
qui
est détectée. Ce détecteur simple, petit et
robuste
permet de détecter des espèces présentes dans le
gaz vecteur à des concentrations comprises entre quelques
parties par million (ppm) et quelques pourcents. Ces
détecteurs ne sont pas destructifs ce qui permet d'envoyer les
gaz issus de la voie analytique vers le spectromètre de masse
pour une seconde analyse des composés.
Photo d'un module
analytique de SAM GC.
En bas, on distingue
le cylindre dans lequel la colonne est
confinée. Sur le dessus, on voit le tube qui sert de
piège d'injection
|

Photo d'un détecteur de SAM GC (TCD).
On voit (en haut et
en bas) les tubes dans lesquels le gaz circule. A droite, les fils
électriques qui permettent d'alimenter le TCD
en courant, et d'acquérir le signal. Sur le dessus du TCD
(flêche
rouge) est placé un capteur
de température
|
La qualité de la
séparation dépend fortement de la qualité de
l'injection du mélange gazeux dans la colonne. Si l'injection
est faite dans des mauvaises conditions, les pics chromatographiques
auront tendance à se recouvrir, ce qui ne permettra pas leur
séparation. Pour s'assurer d'une bonne qualité
d'injection, trois des six voies analytiques sont équipées de
systèmes appelés pièges d'injection. Ces
pièges sont des tubes d'un diamètre de l'ordre du
millimètre remplis de poudre d'adsorbant. A température
ambiante, cette poudre capte les molécules qui traversent le
piège et les retiennent piégées. En chauffant
rapidement le piège, la poudre relache très rapidement
les espèces piégées et l'injection dans la colonne
se fait sur un laps de temps très court, synonyme de bonne
qualité d'injection. Ceci permet également d'augmenter la
sensibilité de la détection.
Ces six voies analytiques existent sous
forme de modules indépendants. Ces modules sont montés
sur une plaque support qui doit être intégrée dans
la structure mécanique de l'expérience SAM.
Le contrôle du
chauffage des différentes parties du chromatographe (colonnes,
détecteurs, pièges) se fait à l'aide d'une
électronique développée par le centre GSFC de la
NASA. L'équipe française a quant à elle
développée l'électronique de contrôle des
détecteurs TCD et d'acquisition de leurs signaux, ce qui
représente une carte électronique de SAM.

Modèle d'ingénieurie de SAM GC.
Les six modules analytiques sont montés sur leur plaque support
(verticale)
|

Carte électronique du modèle dingénieurie de
SAM GC.
Cette carte contrôle les détecteurs de SAM GC (TCD)
|
|
|

